

结直肠癌(Colorectal Cancer, CRC)是全球范围内高发病率与死亡率的恶性肿瘤,其复杂的进展机制涉及多层次的分子网络异常。其中,免疫检查点抑制剂(如抗PD-1/PD-L1抗体)虽为部分患者带来希望,但一个严峻的临床现实是:高达85%的微卫星稳定型(MSS/pMMR)CRC患者对现有免疫治疗基本无响应。这种普遍存在的耐药性,成为提升患者生存率的关键瓶颈。
近日,浙江大学医学院附属邵逸夫医院、中国科学院合肥物质科学研究院等机构的联合研究团队,在国际知名期刊《Molecular Cancer》上发表重要研究成果。他们通过对结直肠癌组织进行深度整合的多组学(转录组、蛋白组、代谢组)分析,首次揭示了一条名为**"LncRNA 60967.1-PLCD4-ATRA"的全新调控轴。该研究不仅阐明了该轴在抑制肿瘤进展和重塑免疫微环境中的核心作用,更关键地是,证明了其激活能有效逆转肿瘤细胞对关键免疫因子IFN-γ的耐药性,并显著增强抗PD-1治疗的疗效。这一发现为破解MSS型结直肠癌免疫治疗困境提供了突破性的新靶点和治疗策略。

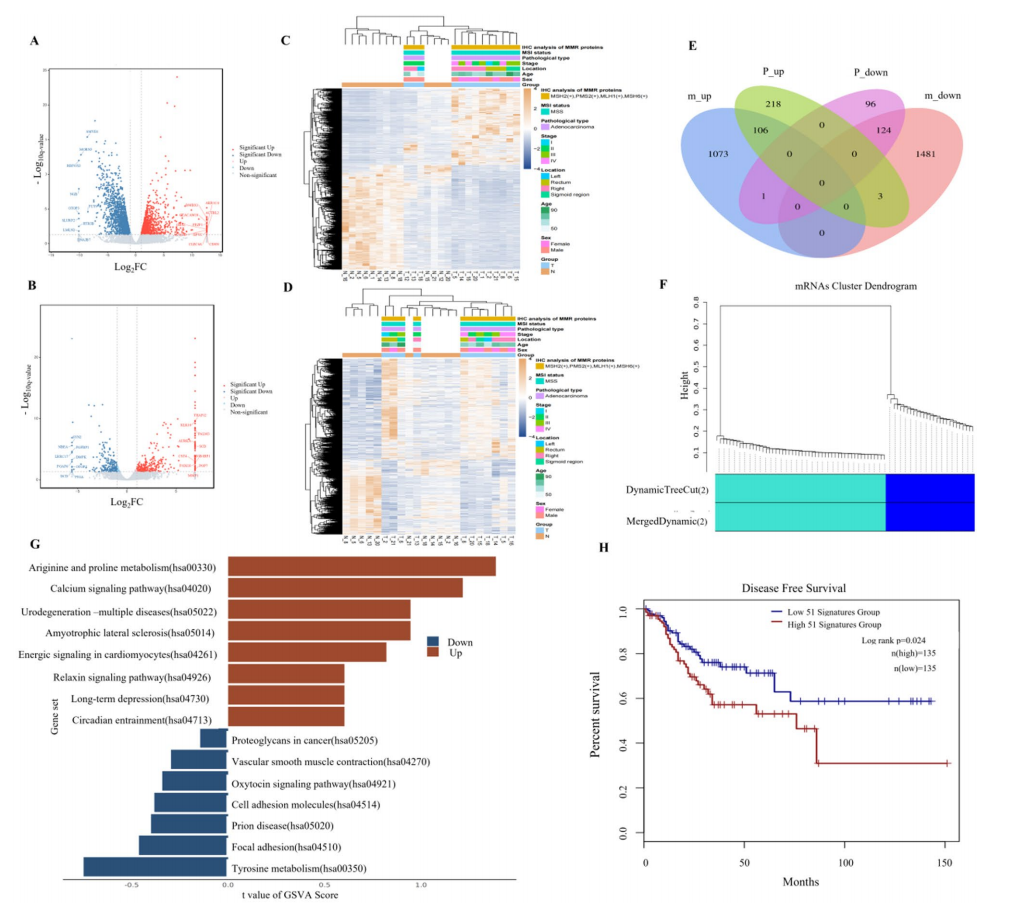
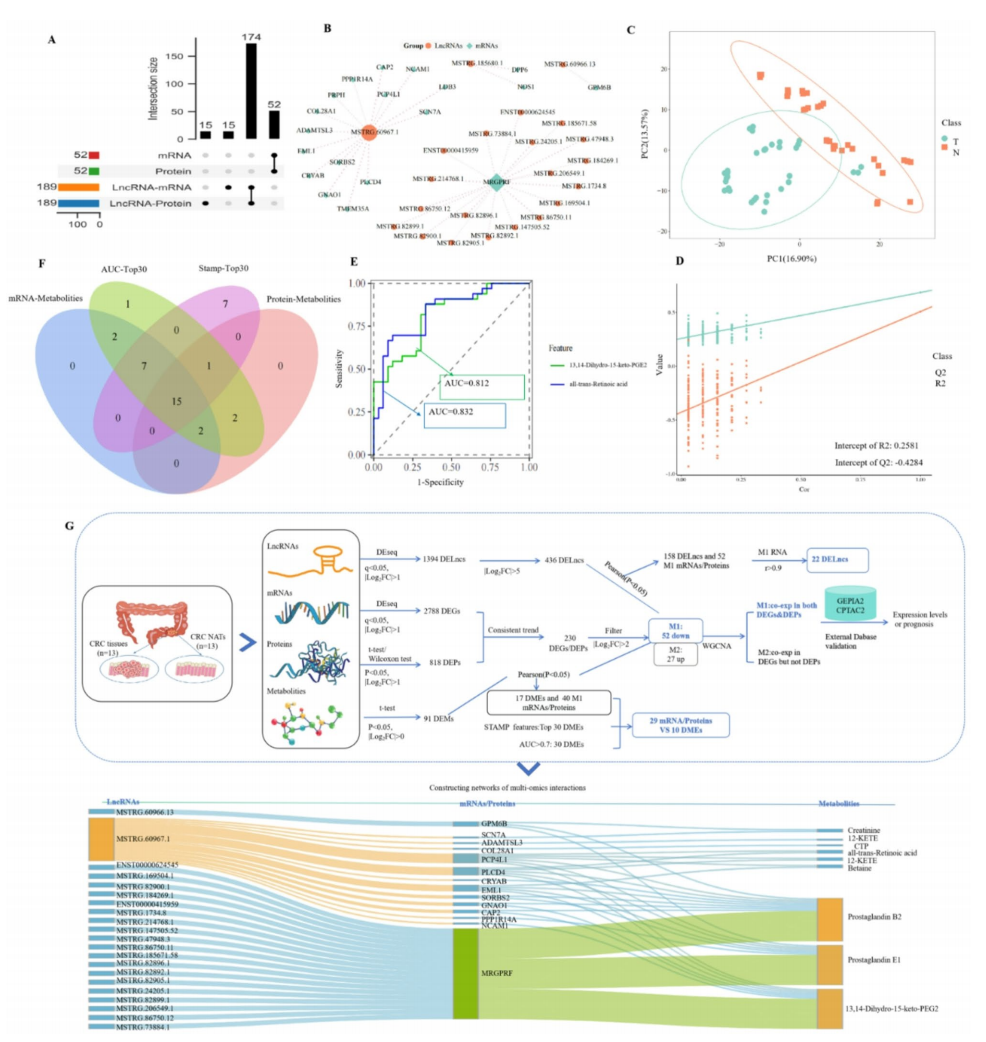
研究团队对13例CRC患者肿瘤/癌旁组织进行转录组、蛋白组、代谢组整合分析。通过WGCNA加权基因共表达网络分析,构建包含1394个差异lncRNA、2788个基因、548个蛋白、91个代谢物的互作网络(图1)。
关键发现:
生物信息学亮点: 采用DESeq2差异分析(q<0.05)、Pearson相关性网络(r>0.9)、模块特征基因筛选(eigengene-traits cor>0.3)锁定关键靶点
通过空间共定位分析(FISH)和RNA-蛋白互作验证(RIP),首次证实:
多组学关联分析:
针对IFN-γ耐药难题,研究通过通路富集分析和受体表达谱解析发现:
功能验证:
基于TCGA-CRC队列(n=650) 的ESTIMATE/xCell双算法验证:
动物模型证据:
(一) 免疫检查点动态调控分析 关键发现:
LncRNA 60967.1过表达显著激活PD-L1免疫检查点通路:
机制解析:RNA-seq结合CUT&Tag分析揭示LncRNA 60967.1通过增强STAT3信号通路促进PD-L1转录
(二) 联合治疗响应模型(CT26/MC38小鼠模型) 治疗方案对比:
治疗组 肿瘤抑制率 体积变化 关键指标 联合治疗 89% -82% CD8+IFN-γ+细胞↑4.3倍
本研究通过整合转录组学、蛋白组学与代谢组学的多维分析,首次构建了结直肠癌"LncRNA-蛋白-代谢物"动态调控网络全景图谱,实现了三大突破性进展:
机制解析突破
发现并验证了 LncRNA 60967.1-PLCD4-ATRA 核心调控轴,阐明其通过上调IFNGR1受体表达逆转免疫耐药的分子机制
技术方法创新
创新性融合 WGCNA共表达网络、ESTIMATE/xCell微环境量化算法及TCGA大数据验证,实现多组学数据的深度耦合解析
临床转化价值
基于动物模型证实该轴激活可使抗PD-1疗效提升112%(抑制率42%→89%),为MSS型CRC的"靶向+免疫"协同治疗提供新范式
这项研究不仅为破解结直肠癌免疫耐药瓶颈提供了全新靶点,更通过多组学联合分析范式,实现了从分子互作网络发现到临床治疗策略设计的全链条突破,为肿瘤精准免疫治疗开辟了创新路径。
本项研究彰显了多组学整合分析在破解肿瘤耐药机制中的核心价值。作为专业的组学技术服务伙伴,谱研生物提供从实验到分析的完整解决方案:
我们提供从「组学实验」→「生信挖掘」→「机制验证」→「临床关联」的一站式服务,助力攻克耐药瓶颈。 原文链接:https://molecular-cancer.biomedcentral.com/articles/10.1186/s12943-025-02359-x
本文由【谱研生物】原创发布,转载请标注来源。
关注公众号,回复"内皮图谱"获取原文!
【联系我们】
谱研生物官方网站:https://www.puyanbio.com/
业务咨询:
